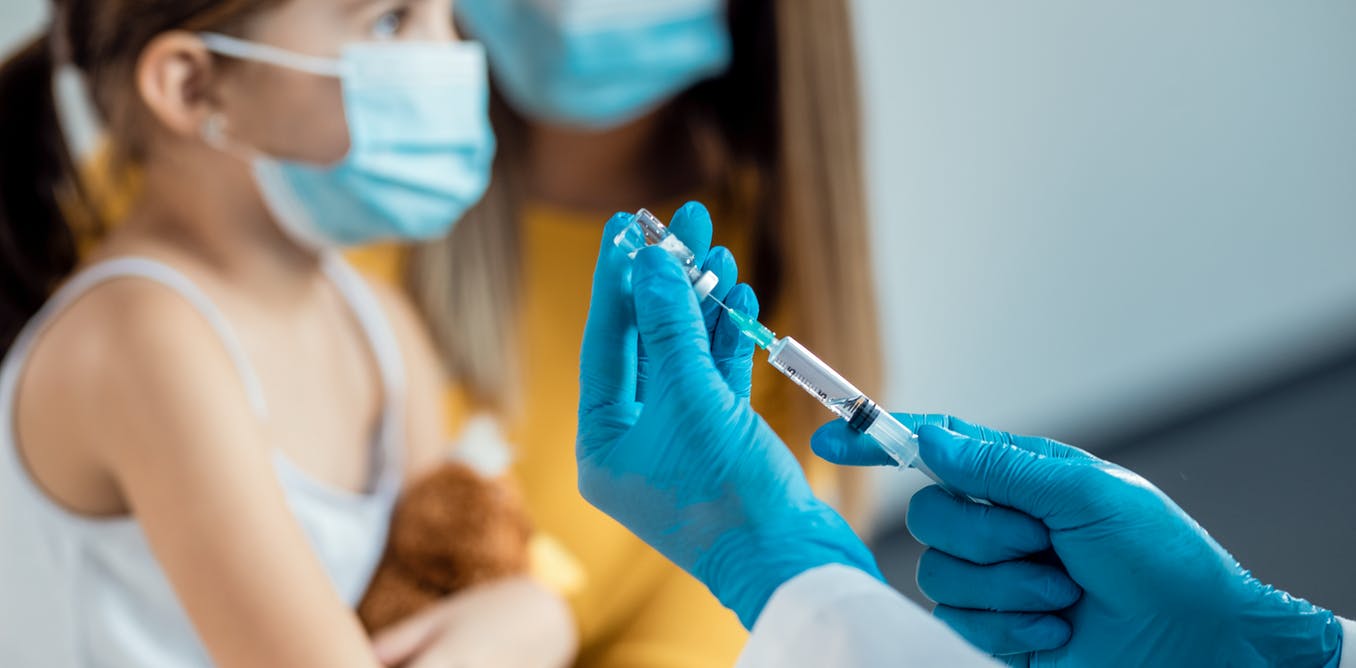
Pfizer dijo el jueves que solicitó formalmente a Estados Unidos la autorización de emergencia para aplicar su vacuna anticovid a niños de entre 5 y 11 años.
Grandes cantidades de niños se han contagiado de la variante delta del coronavirus e inmunizar a la población más joven es considerado un factor clave para mantener abiertas las escuelas y ayudar a terminar con la pandemia.
A fines de septiembre, Pfizer y BioNTech, que desarrollaron juntas la vacuna, comenzaron a enviar datos a la agencia FDA, que supervisa en Estados Unidos los medicamentos, para su muy esperada autorización.
Pfizer dijo el jueves en Twitter que las dos empresas «oficialmente presentaron su pedido a la FDA» para el «uso de emergencia» de la vacuna en niños de 5 a 11 años.
Tras el anuncio, el coordinador de la Casa Blanca para el covid, Jeff Zients, dijo a la cadena CNN que «todos estamos de acuerdo en que contar con una vacuna segura y efectiva para chicos de hasta 11 años es el próximo paso realmente importante en la lucha contra el virus».
En los ensayos, niños de entre 5 y 11 recibieron dos dosis de 10 microgramos con 21 de diferencia entre ambas. Las dos para grupos etarios mayores sobre de 30 microgramos.
La vacuna Pfizer-BioNTech cuenta con la plena autorización de la FDA para los mayores de 16 años.
Vacunación covid-19 a niñas, niños y adolescentes de 12 a 17 años se registra desde el 1 de octubre